Како се прелаз супстанци из течног стања у чврсто стање одвија?
Свака промена у стању материје повезана је са метаморфозом температуре и притиска. Једна супстанца може бити представљена у следећим агрегатним стањима: чврста, течна, гасовита.
Напомињемо да, пошто транзиција није примећенапромене у саставу материје. Прелазак материје из течног стања у чврсто стање прати се само променом снаге интермолекуларне интеракције, распоређивањем молекула. Трансформација из једне државе у другу назива се фазна транзиција.

Таљење
Овај процес укључује трансформацију чврсте супстанце у течност. Захтева повишену температуру.
На пример, у природи можете посматрати таквестање супстанце. Физика лако објашњава таљење снежних пахуљица под утицајем пролећних зрака. Мали кристали леда, који су део снијега, почињу да се разграђују након загревања ваздуха на нулу. Третирање се одвија постепено. Прво, лед абсорбује топлотну енергију. Како се температура мења, лед се у потпуности претвара у течну воду.
Прати га значајно повећање брзине кретања честица, топлотне енергије, повећања вредности унутрашње енергије.
Након постизања индикатора, позовемотемпература топљења, структура чврсте материје је прекинута. Молекули имају већу слободу, они "скокну", окупирају различите позиције. Талирана супстанца има већу резерву енергије него у чврстом стању.

Температура сушења
Прелазак супстанце из течног стања у чврсто стање се јавља на одређеној температури. Ако је топлота уклоњена из тела, она се замрзава (кристалише).
Температура очвршћавања се сматра једним од најважнијих карактеристика.
Кристализација
Прелазак материје из течног у чврсто стањепозиција се назива кристализација. Када се пренос топлоте из течности заустави, температура пада на одређену вредност. Фаза транзиције супстанце из течног стања у чврсту материју у физици се назива кристализација. При разматрању супстанце која не садржи нечистоће, температура топљења одговара индексу кристализације.
Оба процеса поступају постепено. Процес кристализације праћен је смањењем просечне кинетичке енергије молекула садржаних у течности. Снаге привлачности, кроз које се честице држе у стриктном редоследу, инхерентне чврстим садржајима, повећавају се. Након што честице стекну наручени аранжман, формира се кристал.
Укупно стање је физички обликсупстанца, заступљена у одређеном распону притисака и температура. Карактерише га квантитативна својства која се мењају у одабраним интервалима:
- способност супстанце да промени облик и запремину;
- одсуство (присуство) реда дугог или кратког домета.
Процес кристализације је повезан са ентропијом, слободном енергијом, густином и другим физичким количинама.
Поред течности, чврстих материја, гасног облика, произведено је још једно агрегатно стање - плазма. Може се претворити у гасове у случају повећања температуре при константном притиску.
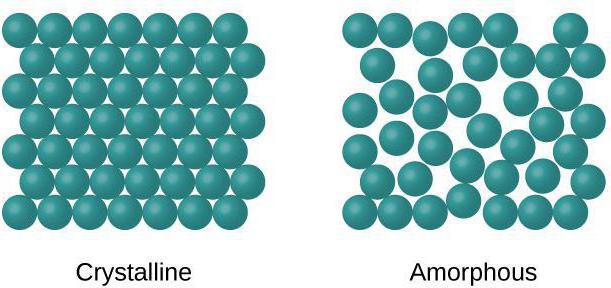
Оквир између различитих стања материједалеко од увек бити стриктан. У физици је потврђено постојање аморфних тела која могу задржати структуру течности која има малу течност. Течни кристали имају могућност поларизације електромагнетног зрачења, који пролази кроз њих.

Закључак
Да би описали различите државе уфизике, применити дефиницију термодинамичке фазе. Критични феномени се називају државама које описују трансформацију једне фазе у другу. Чврсти остаци се разликују очувањем током дужег временског периода њиховог просечног положаја. Они ће направити мање флуктуације (са минималном амплитудом) у близини равнотеже. Кристали имају одређени облик, који ће се променити након преласка у течност. Информације о тачки кључања (таложење) омогућавају физичари да користе практичне сврхе прелазак из једног агрегатног стања у други.



